今回の記事では、高校から大学まで頻出の「酸と塩基の定義」について解説していきます。酸と塩基の定義は1つだけでなく、過去たくさんの人が定義したため、その分だけ覚える必要があります。
この記事を読んで、以下のことを説明できればOKです↓↓
・アレニウスの定義を説明できる
・ブレンステッドの定義を説明できる
・ルイスの定義を説明できる
3つ全てが別の意味を持つ酸と塩基の定義です。そして頻出なので、必ず覚えましょう。さっそくやっていきます。
化学における発見の流れ(飛ばしてOKです)
先に、化学がどのように進むかを理解することで、特に酸と塩基の定義は覚えやすくなります。化学における発見の流れはこのようになっている場合が多いです↓↓
①新しいものを個別のものとして発見する(定義する)
⇒アレニウスの定義(H(+)とOH(-)でそれぞれ定義)
②個別から共通性を発見する(再定義しなおす)
⇒ブレンステッドの定義(H(+)のみで定義する)
③全てのものを、1つの性質に結び付ける(再再定義しなおす)
⇒ルイスの定義(全ての基本である電子で定義する)
今から解説する3つの定義は全てこの順番で発見・定義されています。そのため、この順番を覚えておけば、忘れにくくなると思います。
アレニウスの定義
まずは結論。アレニウスの定義はこれです↓↓
・酸:水溶液中で電離して、H(+)を生じる物質
・塩基:水溶液中で電離して、OH(-)を生じる物質
3つの中で初めに定義されたアレニウスの定義は、酸と塩基を全く別のものとして、「H(+)とOH(-)」によってそれぞれ定義しています。
最初の発見ですので、酸と塩基を個別のもととして定義しました。
反応式で表現すると以下のようになります↓↓
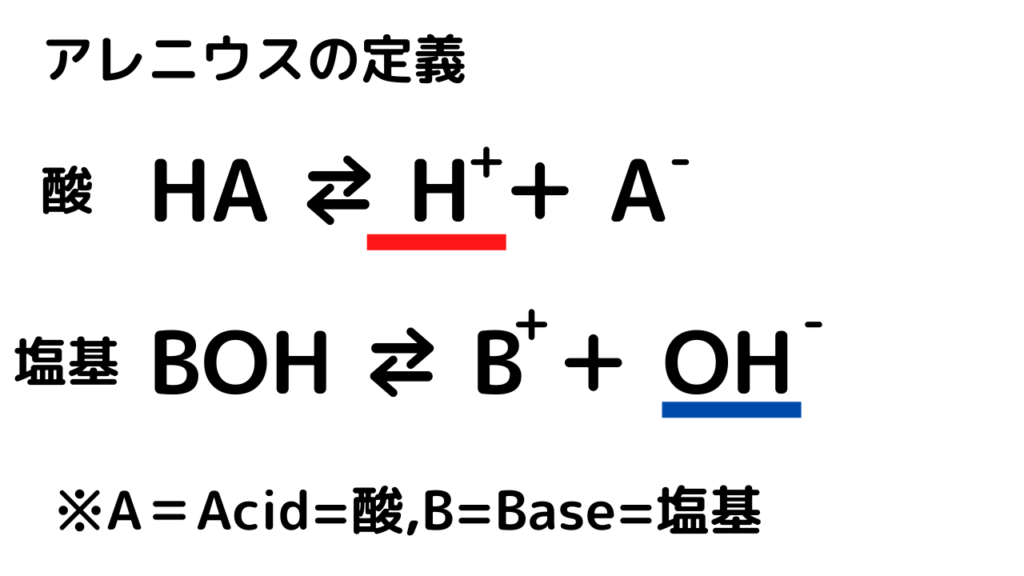
酸と塩基の分野にAとBのアルファベットが使用されることが多いのは、酸を英語でAcid、塩基を英語でBaseなので、その頭文字をとっているからです。
ブレンステッドの定義
まずは結論。ブレンステッドの定義はこれです↓↓
・酸:別の物質へ、H(+)を与えることができる
・塩基:別の物質から、H(+)を受けとることができる
ブレンステッドの定義では、酸と塩基はH(+)の授受によって説明できることがわかり、お互いに関係性があることがわかりました。個別の考えてあったアレニウスの定義から、共通性を発見し、一般化しました。
ここで、H(+)=プロトンという名前があることを覚えておきましょう
そのため、プロトンを与える性質を持つ酸は、「プロトン供与体」と言い、プロトンを受けとる性質を持つ塩基は、「プロトン受容体」と言います。
ブレンステッドの定義において、水H₂Oは酸にも塩基としても定義することができます↓↓
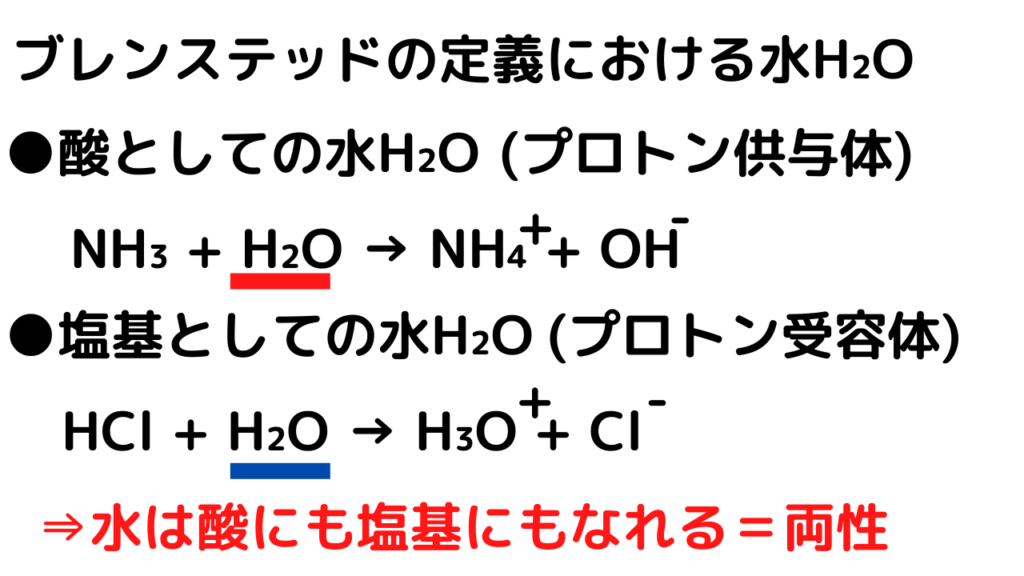
ルイスの定義
まずは結論。ルイスの定義はこれです↓↓
・酸:孤立電子対の受容体
・塩基:孤立電子対の供与体
A + :B ⇄ A:Bとして表現できる
ルイスの定義では、化学物質の基本単位である電子に着目して、発見されました。孤立電子対とは、物質における結合していない電子のことを指しますつまり、非共有電子対のことです。
ルイスの定義はイメージがわきにくいと思いますが、アンモニウムイオンを考えると理解しやすいと思います↓↓
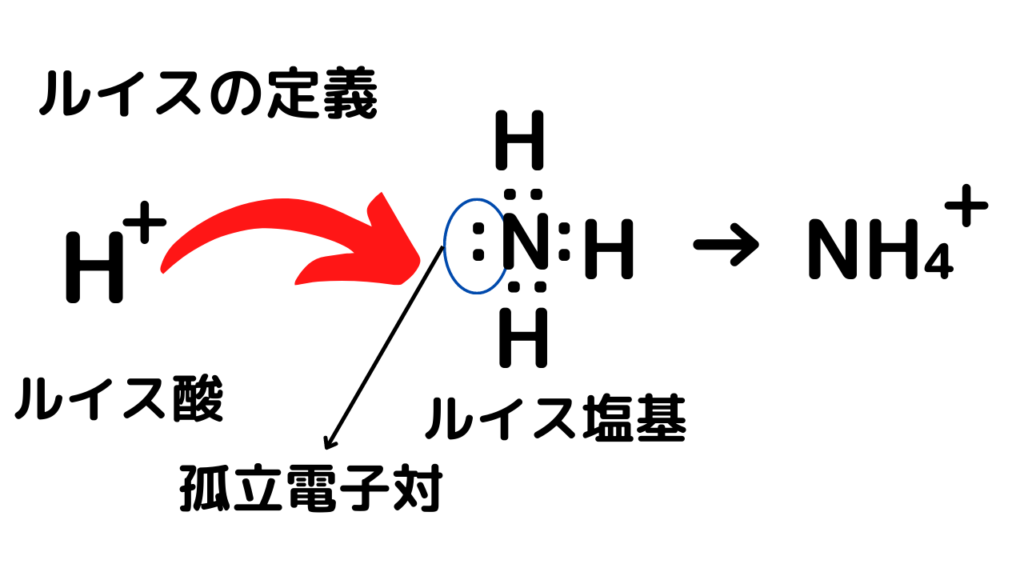
ここでH(+)は孤立電子対の受容体、NH₃は孤立電子対の供与体となっています。(画像ではわかりやすくすため、H(+)を与える形になっていますが…)
これらが酸と塩基の定義で覚える3つです。
以上です。誤りがあればコメント指摘していただけると幸いです。修正します。



コメント