今回の記事では、有機化学で出題される絶対覚えるべき「反応5選」を紹介します。5つ全ての反応が有機化学を支える基礎的な反応なので、ここで確実に覚えましょう!!
今回の記事で以下のことを理解できればOKです↓
・ヨードホルム反応
・銀鏡反応
・フェーリング反応
・アルコールの酸化反応
・アルコールの脱水反応
では、さっそくヨードホルム反応から見ていきましょう。
まずは重要なポイントを押さえましょう↓
・ヨードホルム反応を示す構造を毎回書いて吟味する
・文中に、「ヨウ素」と「水酸化ナトリウム」があったら、ほぼヨードホルム反応
そして、毎回書くヨードホルム反応を示す構造はこれです↓
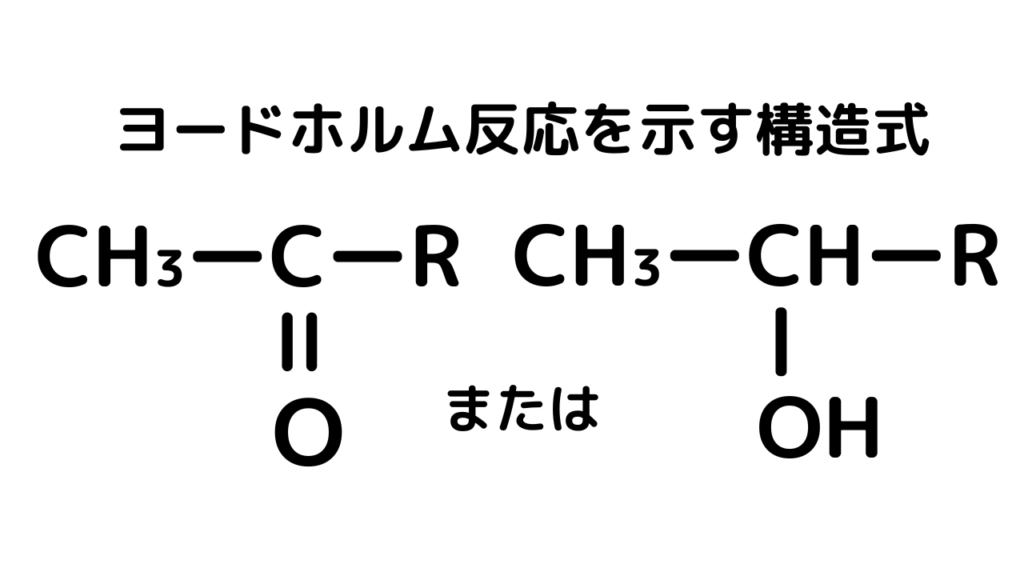
ヨードホルム反応は、ヨウ素と水酸化ナトリウムに上の構造を持つ化合物が関与することで、生成物としてヨードホルムCHI₃ができる反応です。
ヨードホルムCHI₃は特徴のある生成物で、黄色で特有の臭気を持っています。
ここでヨードホルムについて脱線して記述しておきます。
有機化学で17族を扱う際には、名前を変換することが多いです。
フッ素→フルオロ
塩素→クロロ
臭素→ブロモ
ヨウ素→ヨード
最後に、ヨードホルム反応を示す代表的な物質について書いておきます
アセトアルデヒド、アセトン、エタノール、2-プロパノール、2-ブタノールなど
(※これを暗記してはいけません。毎回、示す構造を書いて考えてください)
続いて銀鏡反応について見ていきましょう。
まずは重要なポイントを押さえましょう
・銀鏡反応で、アルデヒド基の還元性の確認ができる
・カルボン酸であるギ酸が、銀鏡反応を示す
アルデヒド基CHOを持つ化合物は、アルデヒド基が持つ性質である「還元性」を有しています。銀鏡反応はその還元性を確認するために行われる反応です。銀鏡反応=還元反応といっていいでしょう。
銀鏡反応で、結果として起こるのは、Ag+がアルデヒドに還元されて銀が生じるということです。
アルデヒド基⇒還元性⇒銀鏡反応と覚えておけばいいですが、注意しなければならない化合物が「ギ酸です」
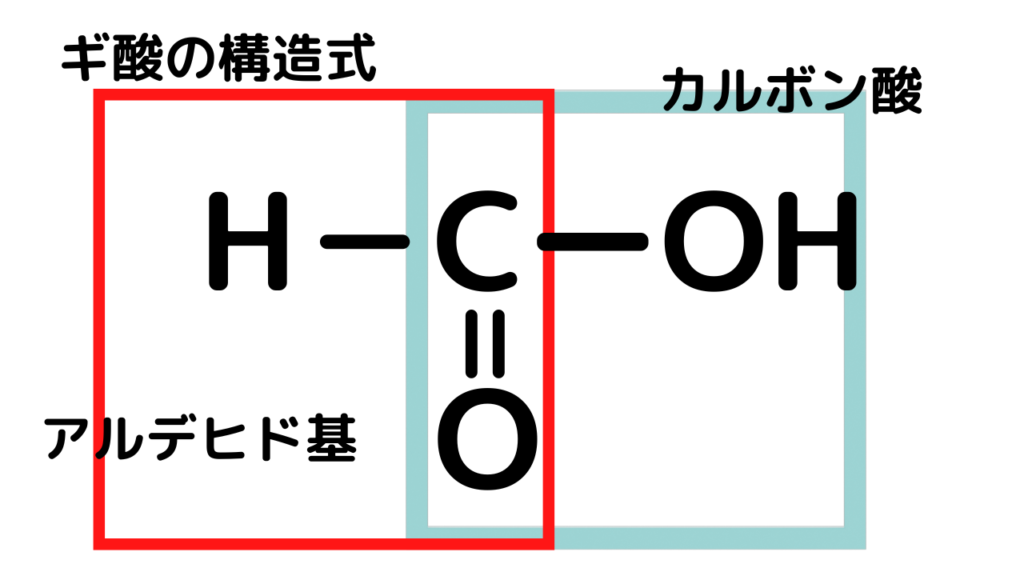
上にあるようにギ酸は名前の通り、カルボン酸に該当する化合物の一種ですが、アルデヒド基を有しています。そのため、銀鏡反応を示す化合物なのです。ギ酸も銀鏡反応に該当する化合物であることを忘れないでおきましょう。
まずは重要なポイントを押さえましょう
・フェーリング反応で、アルデヒド基の還元性の確認ができる
・色の変化(青色→赤色)と物質(Cu(2+)またはCu₂O)を押さえる
アルデヒド基CHOを持つ化合物は、アルデヒド基が持つ性質である「還元性」を有しています。フェーリング反応はその還元性を確認するために行われる反応です。フェーリング反応=還元反応といっていいでしょう。(銀鏡反応と説明は同じ)
フェーリング液で結果として起こることとして、色の変化と物質の変化があります。

最初の液体の色は、青色です。なぜ青色かは、Cu(2+)の色が、青色であるからです。そして、フェーリング反応を起こすと、液体に赤色の沈殿が出現します。これは、Cu(2+)が、アルデヒド基が持つ還元作用によって、酸化銅(Ⅰ)Cu₂Oに変化するからです。沈殿として出現した酸化銅(I)の銅イオンは1価イオンなので注意しましょう。
まずは重要なポイントを押さえましょう
・第1級は2回酸化、第2級は1回酸化、第3級は0回酸化
・酸化の過程で炭素Cの数は変わらないこと
アルコールは第何級に属するかによって酸化の程度が異なります。
第1級アルコール→アルデヒド→カルボン酸
第2級アルコール→ケトン
第3級アルコール→×
アルコールの酸化反応で、必ず出る代表的なのは、メタノールとエタノールです。
①メタノールCH₃OH→ホルムアルデヒドHCHO→ギ酸HCOOH
②エタノールC₂H₅OH→アセトアルデヒドCH₃CHO→酢酸CH₃COOH
①、②の反応は必ず覚えましょう。
①、②を見てわかるように酸化の過程で炭素Cの数が一定です。
①の反応であれば、どんなに酸化しても、メタノールもホルムアルデヒドもギ酸も炭素数は1。②であれば、炭素数は2という具合です。
炭素の数が変わらないと嬉しいことは構造がとりあえずは想像しやすいということです。炭素数1とか2では、あまり実感湧かないかもだけど、6とか7とかになったら、ものすごい効力を発揮します。
まずは重要なポイントを押さえましょう
・温度によって反応が異なる
・濃硫酸は脱水を助けるために使われる
アルコールというか、エタノールについての脱水反応です。
脱水反応には、エタノール1つだけの分子内脱水と、エタノール2つの分子間脱水の2種類存在する
脱水反応はとにかく、温度が大事!と覚えておいてほしい。
160℃~170℃なら、分子内脱水でエチレンC₂H₄を作る
130℃程度なら、分子間脱水でジエチルエーテルC₂H₅-O-C₂H₅を作る
といった具合に、完全に温度に依存しているので覚えておきましょう
まとめるとこんな感じです↓↓
●分子内脱水反応:エタノールC₂H₅OHを1つ使って、脱水。160~170℃という条件のもと、濃硫酸H₂SO₄を触媒として、エチレンC₂H₄を作る
●分子間脱水反応:エタノールC₂H₅OHを2つ使って、脱水。130℃程度という条件のもと、濃硫酸H₂SO₄を触媒として、ジエチルエーテルC₂H₅-O-C₂H₅を作る
そして、濃硫酸は、触媒として、脱水作用を目的に使われている。
脱水反応については、エチレンの記事でも触れているから、確認しておいてほしい↓↓
メタン・エチレン・アセチレン有機化合物(炭化水素)の製法まとめ
以上です。重要な反応なので必ず覚えておきましょう。
誤りがあれば、コメント指摘していただけると幸いです。修正します。




コメント