今回の記事では、有機化学分野の基礎である「官能基」とそれぞれの官能基の覚えておきたい頻出物質について解説します。
この記事を読んで以下のことを理解できればOKです↓↓
・官能基とそれぞれの代表物質の性質が理解できる。
それではアルデヒドから紹介していきます。
アルデヒド基の共通の性質はこちら↓
・R-CHOという官能基を持っている
・還元性を持っている
・第1級アルコールの酸化によって得られる
アルデヒド基を持つ物質は基本的に、以上の3つの性質を持っています。
アルデヒドで覚えておきたい頻出物質は以下の2つです↓↓
①アセトアルデヒドCH₃CHO製法:エタノールの酸化
②ホルムアルデヒドHCHO製法:メタノールの酸化
ケトンの共通の性質はこちら↓
・R-CO-R’という官能基を持っている
・還元性を持っていない⇔アルデヒドとは違う!!
・第2級アルコールの酸化によって得られる
ケトンを持つ物質は基本的に、以上の3つの性質を持っています。
ケトンで覚えておきたい物質は1つだけです↓
①アセトンCH₃-CO-CH₃
アセトンは製法が3つあり、どれも頻出ですので必ず覚えましょう
①酢酸カルシウムの乾留
②2-プロパノールの酸化
➂クメン法の製造過程で得られる
3パターンを詳しく見ていきましょう
①酢酸カルシウムの乾留
(CH₃COO)₂Ca → CH₃-CO-CH₃ + CaCO₃
②2-プロパノールの酸化
CH₃-CH(OH)-CH₃ →CH₃-CO-CH₃
※酸化反応によって、水素が減ることで生成されます。
➂クメン法の製造過程で得られる

また、アセトンはマニキュアの除光液としても使用されます。

アセトンの製法3種類覚えましたか?
エーテルの共通の性質はこちら↓
・R-O-R’という官能基を持っている
・水に溶けにくく、中性の性質を持っている
・単体のナトリウムNaと反応しない⇔アルコールとは違う!!
エーテルを持つ物質は基本的に、以上の3つの性質を持っています。
エーテルで覚えておきたい物質は1つだけです↓
①ジエチルエーテルC₂H₅-O-C₂H₅ 製法:エタノールの分子間脱水(温度:130℃程度)
エタノールの脱水反応については、下の2記事でも触れているのでチェック↓↓
メタン・エチレン・アセチレン有機化合物(炭化水素)の製法まとめ
アルコールの共通の性質はこちら↓
・R-OHという官能基を持っている
・中性の性質を持っている
・低級アルコールは水に溶けやすく、高級アルコールは水に溶けにくい
・単体のナトリウムNaと反応する⇔エーテルとは違う!!
アルコールを持つ物質は基本的に、以上の4つの性質を持っています。
<補足>
・低級アルコールは水に溶けやすく、高級アルコールは水に溶けにくい
低級アルコールと高級アルコールの違いは、「炭素の数」。高級ほど多い
OH基は親水性、Rは基本的には疎水性である
⇒炭素数の少ない低級アルコールは、OH基の影響が大きいので水に溶けやすい
⇒炭素数の多い高級アルコールは、Rの影響が大きいので水に溶けにくい
アルコールで覚えておきたい物質は3つだけです↓
①メタノールCH₃OH 製法:一酸化炭素COに水素H₂(高温高圧、触媒:酸化亜鉛)
CO + 2H₂ → CH₃OH ※条件は高温高圧、触媒は酸化亜鉛
②エタノールCH₃CH₂OH
製法⑴ エチレンC₂H₄に水H₂O
C₂H₄ + H₂O → C₂H₅OH
製法⑵ グルコースの発酵
C₆H₁₂O₆ → 2CH₃CH₂OH + 2CO₂
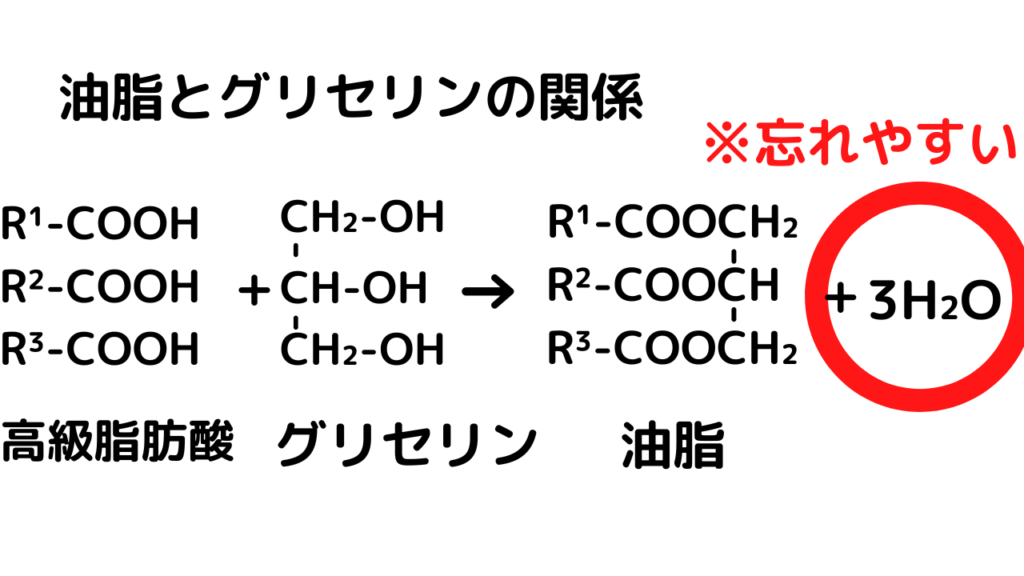
③グリセリン:油脂でめちゃくちゃ出題される重要な物質
カルボン酸の共通の性質はこちら↓
・R-COOHという官能基を持っている
・アルデヒドの酸化によって得られる
⇒第1級アルコール→アルデヒド→カルボン酸
カルボン酸を持つ物質は基本的に、以上の2つの性質を持っています。
カルボン酸で覚えておきたい物質は4つです
①ギ酸HCOOH 製法:ホルムアルデヒドの酸化 ※還元性あり
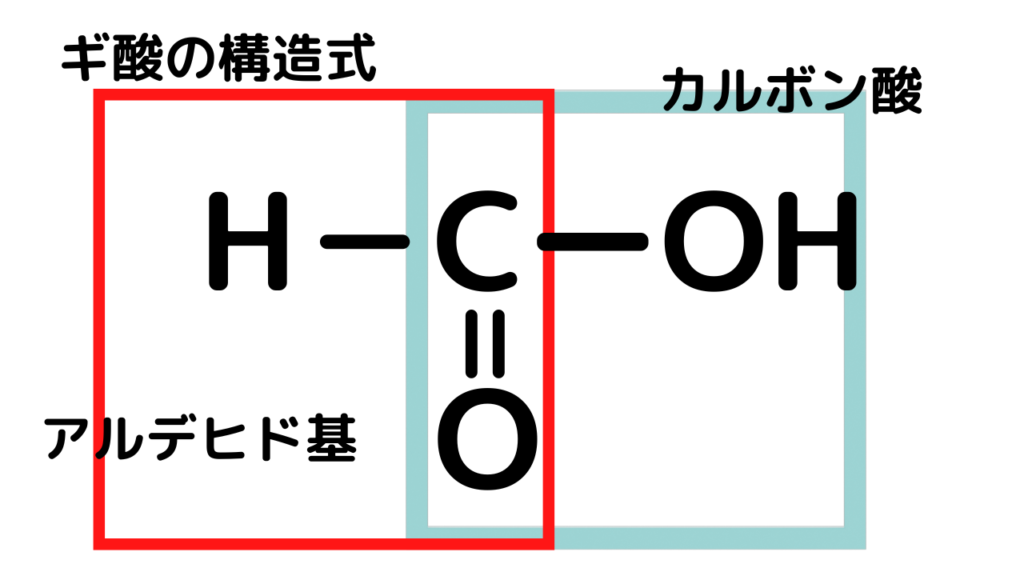
上の画像からギ酸は還元性を示すアルデヒド基を持っていることがわかります。
②酢酸CH₃COOH 製法:アセトアルデヒドの酸化
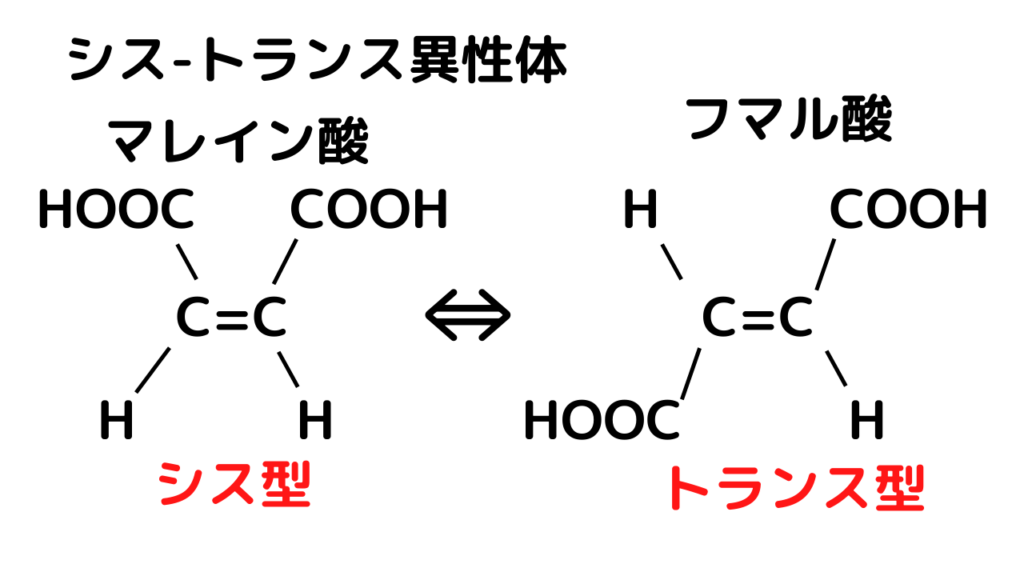
③マレイン酸 HOOC-CH=CH-COOH シス型
④フマル酸 HOOC-CH=CH-COOH トランス型
※③、④は、シスートランス異性体の関係にある。
以上です。誤りがあればコメント指摘していただけると幸いです。修正します。




コメント